2022-08-08 462
西奈山大学的研究人员对人类小胶质细胞(驻留在大脑中的免疫细胞)的遗传和分子机制取得了前所未有的了解,这可能为它们如何促进阿尔茨海默病(AD)的发展和进展提供宝贵的见解。该团队的研究结果发表在《自然-遗传学》杂志上。
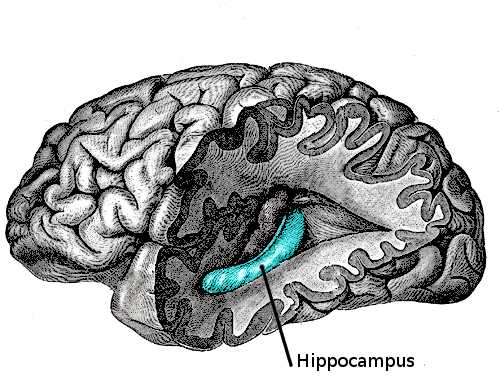
通过对150名捐赠者的活体组织活检或解剖,研究人员确定了21个候选风险基因,并强调了其中一个SPI1,作为小胶质细胞和AD风险的潜在关键调节因子。
“我们的研究是迄今为止最大的人类新鲜组织小胶质细胞分析的遗传风险因素,可能会使人易患阿尔茨海默病,”资深作者帕诺斯·鲁索斯说,他是医学博士,医学博士,精神病学、遗传和基因组科学教授,在西奈山伊坎医学院和疾病神经基因组学中心主任。“通过更好地理解小胶质细胞功能相关的分子和遗传机制,我们就能更好地解开控制该功能并导致AD的调控格局。”反过来,这些知识可以为一种目前没有有效治疗方法的疾病的新治疗干预铺平道路。”
小胶质细胞主要负责大脑中的免疫反应,对神经元的发育和维持也至关重要。尽管包括西奈山大学(Mount Sinai)的一些研究在内的先前研究已经确认,小胶质细胞在阿尔茨海默病的遗传风险和发展中发挥着关键作用,但人们对这一过程的表观遗传机制知之甚少。由于在人脑中分离小胶质细胞具有挑战性,以往的大多数研究都使用了基于动物或细胞系的模型,这些模型不能反映大脑中小胶质细胞功能的真正复杂性。另一个挑战是将AD的遗传风险变异与特定的分子功能联系起来,因为这些风险因素经常出现在基因组的非编码部分(过去被称为“垃圾DNA”),这更难研究。
西奈山研究小组的解决方案是,通过四个大脑生物存储库(三个在西奈山,另一个来自拉什大学医学中心/拉什阿尔茨海默病中心)的合作,从活体组织或尸体解剖中获取新鲜的脑组织。Roussos博士解释说:“使用来自这些来源的150个样本,我们能够分离出高质量的小胶质细胞,这通过反映健康和神经退行性疾病患者小胶质细胞的整套调控成分,为基因调控提供了前所未有的见解。”
这一过程——比较AD和健康老年患者样本的表观遗传、基因表达和遗传信息——让研究人员全面描述了人类小胶质细胞功能是如何通过基因调控的。作为统计分析的一部分,他们扩大了之前全基因组关联研究的发现,将识别出的易患ad的遗传变异与特定的DNA调节序列和基因联系起来,这些基因的调节失调被认为直接导致了疾病的发展。他们进一步描述了细胞范围内的调控机制,作为一种识别基因区域的方式,涉及到小胶质细胞活动的特定方面。
通过他们的研究,科学家们对SPI1基因有了新的认识,SPI1基因是主要的小胶质转录因子,调节着与AD基因相关的其他转录因子和基因的网络。研究小组获得的数据对于破译其他神经退行性疾病(包括帕金森病、多发性硬化症和肌萎缩性侧索硬化症)背后的分子和基因奥秘也很重要,小胶质细胞在这些疾病中发挥了作用。
鲁索斯博士承认,他的团队还有很多工作要做,要完全了解这些被识别的基因是如何促进阿尔茨海默病的发展和进展的,以及如何用新的治疗方法来针对它们。尽管如此,他的小神经胶质细胞实验室使用高度复杂的仪器对单细胞进行分析,结果发现了大脑中不同类型的免疫细胞与其外围之间独特的相互作用,这些相互作用与神经退行性疾病有关,这让他深受鼓舞。“通过单细胞数据,我们看到了非常令人兴奋的结果,”鲁索斯博士报告说,“这让我们更接近于理解遗传疾病(如阿尔茨海默病)的基因驱动变异和细胞特异性相互作用。”
原文链接:http://www.yoodor.cn/blog/145.html
=========================================
http://www.yoodor.cn/blog/ 为 “试药博客” 唯一官方服务平台,请勿相信其他任何渠道。
分类一 2022-07-12
分类二 2022-07-24
分类一 2022-07-12
分类一 2022-07-25
分类一 2022-07-26
分类一 2022-08-05
分类一 2022-08-08
分类一 2022-07-12
分类一 2022-07-12
分类二 2022-07-23
扫码二维码
获取最新动态
